
编者按
自2012年基因编辑技术被发现以来,一直被认为是药物发现的转折点。事实上,CRISPR基因编辑技术具有前所未有的能力,可以通过系统地测试靶向基因改变的细胞效应来探究疾病的机制基础。特别是,癌症特有的疾病特征,很容易被大规模并行的CRISPR基因筛查所利用。在这些筛选中,与同一测试池中的其他细胞相比,携带指导RNA的单个细胞也可以作为感兴趣的DNA编辑的条形码,可能会获得竞争性或减少的增殖优势。癌症细胞系(CCLs)和癌症衍生组织中产生的基因图谱现在支持新药开发合理化的异常速度和经济性,并可能缩短试验台到试验台的时间。
今天,我们分享德克萨斯大学西南医学中心、加州大学圣地亚哥分校、多伦多大学Jason Moffat研究团队发表在Science的一项研究——“Impact of CRISPR in cancer drug discovery”,该研究阐述了基因编辑技术在癌症药物发现中的巨大作用,强调了精确的基因编辑可以大规模地平行识别促进癌症的基因。基于CRISPR基因编辑技术的癌症细胞系筛选,以及细胞生长等表型读数,可以促进发现可能成为治疗靶点的基因相互作用,这些数据集和其他信息的机器学习可用于模拟药物对肿瘤微环境的影响,并更好地预测对患者的影响。
文章题目
Impact of CRISPR in cancer drug discovery
杂志:Science(IF=44.7)
发表时间:2024年10月24日
作者:Jason Moffat, Alexis C. Komor,Lawrence Lum Authors Info & Affiliations
单位:德克萨斯大学西南医学中心、加州大学圣地亚哥分校、多伦多大学等
01、研究成果
当观察到的给定双突变体(在同一基因或两个不同基因中包含两个突变的癌症细胞)的适应度表型偏离基于两个单突变体表型之和的预期表型时,就会发生遗传相互作用(GI)。如果双突变体的增殖比预期的要好,则该基因对被认为表现出阳性GI。相反,阴性GI与增殖缺陷有关,增殖缺陷比单基因突变效应预期的更严重。这可以从合成疾病(细胞存活率降低)到最极端的合成致死性(细胞死亡)。合成致死性GIs代表了一个挖掘不足的潜在靶点来源,并基于癌症基因依赖图谱获得了关注,该图谱是使用CCL中的大规模单基因扰动屏幕构建的。此外,假设与癌症细胞中观察到的相比,正常组织的健康对此类GI的依赖程度较低,则此类机会有可能支持创建具有更大治疗窗口(具有可耐受毒性的有效药物剂量范围)的药物。
GI概念可以扩展到给定表型的许多突变相互作用,因此即使在CRISPR基因编辑技术的帮助下,也能迅速超越人类细胞中任何系统实验方法的极限。与此同时,推理或机器学习方法可以帮助填补这些空白。事实上,目前的目标就是使用机器学习模型创建个性化治疗,这些模型参考CCL表型数据库(如DepMap)和从肿瘤中检索的基因组序列信息来预测药物反应。尽管在肿瘤学领域,基于癌症细胞适应度和增殖,GIs通常与合成致死性相关,但在专注于其他适应表型(如胚胎和成人发育)的遗传学观察中,出现了GIs的证据。
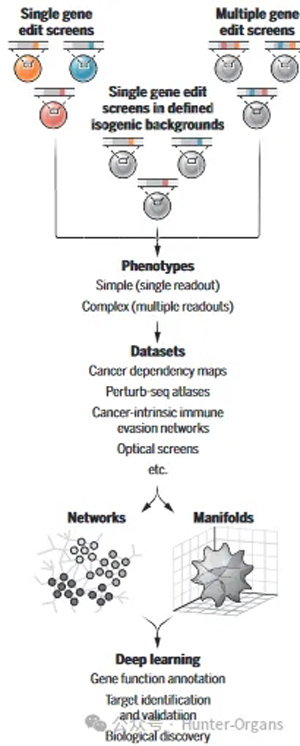
图1 基因编辑技术可用于探索药物靶标
此外,作者指出,还可以使用串联基因CRISPR微扰技术对GI进行编目,该技术可以识别单基因消除方法无法识别的潜在药物靶点。这些筛查解决了重要的生物学问题,包括CRISPR基因编辑技术介导的DNA损伤反应对筛查结果解释的不利影响;冗余基因(paralogs)的作用,可能使癌细胞能够承受任何一个paralogs基因的缺失;以及发现可作为治疗靶点的GI。使用这种串联基因扰动筛选出现的药物开发新机会包括DUSP4/6(双特异性磷酸酶4和6)酶,这些酶被证明可以共同促进突变NRAS(神经母细胞瘤ras病毒癌基因同源物)或BRAF(B-Raf原癌基因,丝氨酸/苏氨酸激酶)的致癌活性。鉴于在整个基因组中生成数据矩阵需要大量的组合双基因扰动排列,针对有限数量的特定基因类(如转录因子或磷酸化酶)的CRISPR基因编辑文库应有助于实现组合基因扰动事件的饱和水平,从而提高这些具有挑战性的筛选中的基因覆盖率(图1)。
识别GIs的另一种方法是建立含有癌症相关突变的等基因(其他基因相同)细胞系,并用全基因组微扰库对其进行筛选,以推断GIs。这种方法的优点是,可以精确定义与癌症相关的常见突变——查询,并在实验室之间共享细胞系以进行后续研究。这种等基因方法是使用基于全基因组RNA干扰的筛查开创的,该筛查通过靶向信使RNA进行降解来沉默基因表达。最近,这种方法已被用于使用全基因组CRISPR筛选来鉴定与脂肪酸代谢相关的GI,并正在积极研究作为治疗靶点。
类器官捕获了完整肿瘤的重要特征,这些特征在CCL中经常丢失。它们是由自我更新的细胞产生的,这些细胞保留了不断细化二次细胞类型的能力。因此,在类器官中使用CRISPR基因编辑技术选择性耗竭潜在的抗癌靶点可以产生复杂的表型,更精确地捕捉具有完整细胞结构的肿瘤中靶点失活的影响。类似地,应用于类器官(或三维细胞培养中的癌症细胞系)的大规模平行基因筛选可以提供一种方法来识别在更多生理条件下支持癌症细胞行为的基因。因此,此类类器官筛查有可能鉴定出在典型CCL培养条件下未报告的基因。然而,在这些更具挑战性的生长环境下(即使用细胞外基质支持、更专业的培养基配方)执行基因组规模筛查的困难限制了联合体生成类似CCL的全面遗传数据库的机会。在体内进行的CRISPR基因编辑筛选也被证明是揭示癌症进展调节剂的一种强大方法,这些调节剂不一定在癌症中发现,而是在宿主细胞中发现。
CRISPR基因编辑技术能够快速、系统地说明癌细胞的选择性遗传脆弱性,既有癌症类型依赖性的形式,也有合成致命相互作用的形式,这促使药物开发人员将新的遗传观察结果与在患者中产生类似选择性反应的治疗剂相匹配。因此,代表非典型或难以培养的细菌靶点的基因,如决定细胞类型的转录因子,在对这些基因在癌症中的功能有更大信心的基础上,加倍努力开发药物。然而,嵌入未来药物开发中的CRISPR基因编辑技术平台也可以通过大规模并行基准测试靶向和靶外效应来加速基因到药物的时间线,以识别意想不到的机会或威胁。
此外,碱基和引物编辑技术的出现使得能够系统地评估药物活性,以对抗编码已验证癌基因和肿瘤抑制因子的整个基因序列中的靶向碱基对置换,从而了解癌症中潜在的先天性和所需的抗药性突变,以及患者对给定药物的反应可能性。尽管本文没有讨论,但基于CRISPR基因编辑的疗法也可能被用来解决以前难以治疗的药物靶点,这些靶点不适合更传统的基于小分子的方法。
因此,尽管CRISPR基因编辑生成的功能目录缩短了识别潜在药物靶点的时间,但CRISPR衍生技术的持续进化对于将这一新发现的知识转化为下一代药物至关重要。
作为健康美丽产业CRO服务开拓者与引领者、斑马鱼生物技术的全球领导者,环特生物搭建了“斑马鱼、类器官、哺乳动物、人体”多维生物技术服务体系,开展健康美丽CRO服务、科研服务、智慧实验室搭建三大业务。目前,环特已建立200多种斑马鱼模型,胃癌、脑类器官、心脏类器官及各种肿瘤类器官培养平台,欢迎有需要的读者垂询!
