2024年3月14日,第19个世界肾脏日。权威医学期刊《柳叶刀》最新研究数据显示,目前全球慢性肾脏病患病者超过8.5亿人,我国慢性肾脏病患病率也已超过10%,然而,由于慢性肾脏病早期没有明显的症状,不易察觉,因此被称为“沉默的杀手”。
近年来,随着斑马鱼、类器官、基因编辑等技术的发展及相互结合、互为补充,它们为肾脏研究提供了更加接近真实肾脏的模型生物及体外模型,成为研究肾脏发育、疾病机制及药物筛选的3大利器,为深入了解肾脏发育、肾小球疾病、急性肾损伤( AKI)、肾脏再生、多囊性肾病等疾病机制,为肾脏疾病的预防和治疗提供了新的策略和方法,具有广泛的应用前景和巨大的潜力。
01、斑马鱼在肾脏研究中的应用
近年来,斑马鱼作为一种新型的模式动物,其生理、发育、代谢与哺乳类动物高度相似,基因与人类基因同源性达87%,能可靠模拟和预测人类生理、病理过程,因此,其在肾脏研究中的应用日益广泛。而将斑马鱼与基因编辑技术结合应用,又进一步推动着肾脏研究的进展,为肾脏疾病的预防、诊断和治疗提供了全新的视角和可能性。其在肾脏研究中的应用进展主要包括以下几个方面:
用于肾脏发育及再生机制研究
由于斑马鱼的肾脏具有再生能力,因此其已成为研究肾脏发育及再生机制的重要工具。通过修改斑马鱼基因来研究特定基因对肾脏发育与再生的影响,观察斑马鱼肾脏发育及再生过程,揭示肾脏再生的关键分子和信号通路,不仅有助于了解肾脏发育、再生机制及疾病发生机理,还为开发新的肾脏疾病治疗方法提供了重要的实验模型与理论基础。
研究对象:发现肾脏再生的“刹车”分子
2023年11月7日,陆军军医大学刘赤研究员、赵景宏教授、黄英辉教授团队在Nature Communications发表最新研究成果,该研究通过构建斑马鱼AKI模型,发现在斑马鱼肾小管近端特异表达的脑啡肽原(Proenkephalin-A),能剂量依赖性的抑制肾脏再生的启动因子过氧化氢(H2O2)的产量,进而影响肾脏祖细胞间质上皮转化的关键基因tcf21启动子H3K4me3修饰的重塑,从而控制肾脏再生的强度以及终止;
研究人员又利用基因编辑技术构建了斑马鱼penka突变体,发现PENK-A表达缺失会加速肾脏再生,提示PENK-A对肾脏再生具有负调控作用。

来源:Chi Liu,Xiaoliang Liu,Zhongwei He,Proenkephalin-A secreted by renal proximal tubules functions as a brake in kidney regeneration.Nature Communications,2023.11
用于评价药物的肾脏毒性
肾脏是人主要的排泄器官,也是药物毒性累积并引发急性损伤的靶器官。作为优良的药物肾脏毒性评价模型,斑马鱼具有诸多优势,如繁殖速度快、高通量筛选、与人类肾脏高度相似等,不仅可以通过显微或病理切片观察是否形成肾包膜水肿等肾脏异常、评价肾脏损伤情况,也可以通过测定肾小球滤过率、观察肾小管和肾单位的形态变化等,更准确地评估药物的肾脏毒性,为药物的安全性评价提供有力支持。
研究对象:药物对斑马鱼肾脏毒性的作用机制
Gorgulho等人通过斑马鱼模型评价10%的庆大霉素、扑热息痛和替诺福韦对肾脏的影响,结果显示庆大霉素和扑热息痛可以降低肾清除率,扑热息痛和替诺福韦扩大近端小管,其肾毒性机制与线粒体改变有关,包括变形、线粒体肿胀、嵴断裂和(或)基质颗粒丢失。
Hentschel等通过构建斑马鱼急性肾损伤模型评价药物肾毒性,在50、72hpf的斑马鱼胚胎心脏静脉窦内注射庆大霉素或顺铂引起严重的肾小管重吸收功能障碍;王雪等在利用转基因斑马鱼研究马兜铃酸的肾毒性时,发现马兜铃酸经40~80μmol/L处理后,斑马鱼出现肾小球囊性膨胀、结构疏松、前肾管上皮细胞细胞排列松散、紊乱及管腔扩张样改变等情况,经qPCR检测发现20μmol/L马兜铃酸处理24h后nephrin蛋白(nephrin表达于肾小球足细胞,其与裂孔隔膜的形成相关)表达显著降低,表明马兜铃酸诱发肾损伤的原因可能是肾小球足细胞的功能变化。
来源:李红燕,谢 倩,王 成,李金秀,马 荣,任敉宏,李 勇,王佳俊,陈 海,王 建. 斑马鱼在药物毒理学评估中应用及机制的研究进展 [J]. 中草药, 2021, 52(1): 278- 288.
用于急慢性肾病类药物研发
斑马鱼可用于急慢性肾病类药物研发,通过比较不同药物对斑马鱼肾脏损伤的治疗效果,筛选出具有最佳疗效的药物,也被用于筛选具有肾脏保护作用的药物或具有辅助功效的功能性食品,有助于加速药物或功能性食品研发进程,为临床治疗及消费者提供更多有效的选择。
近年来,在肾脏疾病治疗领域中涌现了多个具有肾脏保护的新型药物,如钠-葡萄糖协同转运蛋白 2 抑制剂(SGLT-2i)、非奈利酮、布地奈德迟释胶囊、血管紧张素脑啡肽酶抑制剂(ARNI)类药物等。
研究人员通过在胚胎斑马鱼中给予马兜铃酸 (aristolochic acid, AA) ,确定了三种可减弱HF的化合物:丝裂原活化蛋白激酶1(MEK-1)、查耳酮衍生物C25和酚类化合物A11。另一项使用相同AA诱导HF模型的研究表明,使用恩格列净(一种钠-葡萄糖协同转运蛋白2(SGLT2)抑制剂),可用于治疗II型糖尿病和HF,减弱心脏形态变化,并降低ANP和BNP基因表达及胚胎斑马鱼的死亡率。
来源:Shi X, Verma S, Yun J, et al. Effect of empagliflozin on cardiac biomarkers in a zebrafish model of heart failure: clues to the EMPA-REG OUTCOME trial?[J]. Molecular & Cellular Biochemistry, 2017.
02、类器官在肾脏研究中的应用
近年来,随着干细胞生物学及基因编辑等技术的进步,肾脏类器官的研究进展突飞猛进。通过体外培养产生的具有三维结构的微型肾脏模型,即“肾脏类器官”,不仅可以模拟肾脏的复杂结构和功能,构建疾病模型,从而研究肾脏肿瘤机制及治疗方法,还可以用于药物筛选、毒性测试,甚至可能最终应用于临床移植。
用于肾脏发育和疾病机理研究
研究对象:探索建立高质量的肾脏收集管的类器官模型,使肾单元与收集管之间建立连接,助力实现从微型肾脏类器官模型向合成人工肾的飞跃。
2021年6月15日,美国南加州大学凯克医学院博徳干细胞研究所李中伟团队在Nature Communications杂志上发表最新研究成果。该研究首次报道了一种全新的三维培养方法,能够以类器官的形式对人和小鼠的原代收集管祖细胞,或者由人类多能干细胞 (hPSC) 分化而来的收集管祖细胞进行体外培养、扩增、并最终诱导分化为成熟的收集管。该系统为利用干细胞合成人工肾提供了重要的集合管祖细胞作为元件;并结合基因编辑技术,该体外诱导的收集管类器官模型可广泛应用于肾脏发育和疾病机理研究。
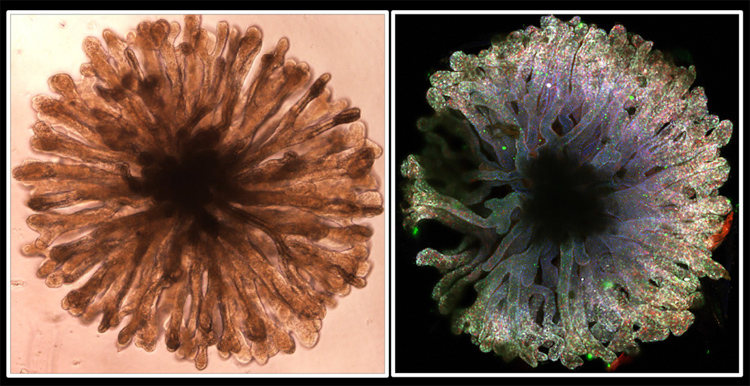
左图:显微镜下的呈现分支状的新型肾脏集合管类器官模型。右图:新的肾脏集合管类器官模型能够在体外模拟成体肾脏的集合管的两类功能性细胞群:principal cell (红色)和intercalated cell (绿色)。
作为结构和组成最复杂的器官,肾脏的损伤和相关疾病一直是困扰人类健康的重大问题。李中伟团队的本项成果为研究肾脏的发育、疾病和再生提供了重要的类器官研究平台。这一系统将极大的推动肾脏的发育生物学和病理学研究,并为进一步的体外人工合成肾脏提供了关键的原材料。
来源:http://doi.org/10.1038/s41467-021-23911-5
用于肾脏疾病药物筛选
研究对象:利用人类肾脏类器官模拟了从内在修复到不完全修复的转变,筛选发现具有治疗肾脏疾病的药物。
一直以来,以内在修复为特征的急性肾损伤到不完全修复和慢性损伤的转变很难开展研究。2022年3月,麻省总医院的Ryuji Morizane团队在Science Translational Medicine上发表题为“Modeling injury and repair in kidney organoids reveals that homologous recombination governs tubular intrinsic repair”的文章,该研究利用人类肾脏类器官模拟了从内在修复到不完全修复的转变。通过单次暴露于顺铂导致内在修复,保留了管状结构和与同源定向修复相关的基因上调。然而,随着顺铂反复暴露,FANCD2和RAD51重组酶被下调,导致修复不完全。
研究人员利用靶向药物筛选确定了DNA连接酶IV抑制剂SCR7可通过增加FANCD2介导的修复,帮助改善类器官中慢性损伤的进展,这表明靶向FANCD2/RAD51途径可能具有治疗肾脏疾病的潜力,同时也进一步证明肾脏类器官在探究潜在疗法中的重要作用。

用于罕见遗传性肾病等研究
研究对象:RAAS 缺陷类器官揭示血管生成延迟可能是常染色体隐性肾小管发育不全的病因。
常染色体隐性肾小管发育不全(AR-RTD)是一种罕见、严重且常导致死亡的疾病,其特征是患者体内与肾素-血管紧张素-醛固酮系统(RAAS)相关基因发生致病性变异,导致近曲小管(PT)完全缺失或严重减少。2023年4月,美国辛辛那提大学医学院的一项最新研究发现,AR-RTD可能主要是由于血管生成延迟所致。这项研究通过使用诱导多能干细胞(iPSC)分化为肾类器官,并进行移植和血管化,探索AR-RTD中PT病理的可能机制,为深入了解AR-RTD的病因提供了新的线索,也为相关疾病的治疗提供了新的思路。

来源:10.1038/s41467-023-43795-x.
用于肾脏药物药效及毒性评价
研究对象:构建一种可量化的基于人肾类器官的方法,应用于临床前评估靶向人肾小球足细胞的药物。
足细胞对肾脏过滤屏障至关重要,其损伤导致许多肾脏疾病,包括局灶性节段性肾小球硬化症(FSGS),这是最常见的与CKD相关的组织病理学原因。GFB-887是一种新型的小分子药物, 可靶向瞬时受体电位通道TRPC5,抑制其激活。2022年7月,Science Advances上发表了一篇题为《Transplanted organoids empower human preclinical assessment of drug candidate for the clinic》的最新研究成果。
在本研究中,研究人员开创了一种利用移植的人肾脏类器官进行动物体内PD研究的新方法。通过移植类器官来实现类器官的成熟和血管化,使药物能够以足够高的浓度输送到移植类器官的生物体内,并利用体外生长的类器官进行了环孢素A(临床常用的肾脏病药物)和GFB-887(TRPC5的新型小分子抑制剂)的药效比较实验,证明了人源类器官可用于临床前PD研究。这种新方法是可重复,可量化的,其可靠性得到了充分验证。

来源:10.1126/sciadv.abj5633
守护肾脏健康,优化用药实践!斑马鱼、基因编辑及类器官技术等,为肾脏病的治疗、药物发现及机制研究等提供了新的可能性。环特生物依托于斑马鱼+哺乳动物+类器官+基因编辑4大技术平台,基于过去10余年持续的技术创新实践,以专业、前沿的技术服务解决方案,助力科研人员在肾脏病研究与治疗上取得更多突破,共同为人类肾脏健康事业做出更大的贡献!
【业务合作咨询】:成先生 17364531293(微信同号)

